Søgeord:NAD+,53-84-9,NAD+ bioaktivt peptid
NAD+, forkortelsen af Nicotinamide Adenine Dinukleotid, er et livsvigtigt coenzym, der findes i alle levende celler i den menneskelige krop, og er også det kernemolekyle, der forbinder cellemetabolisme, DNA-reparation, ældningsregulering og sygdomsforekomst. Siden opdagelsen i 1904 er NAD+ blevet bekræftet at deltage i mere end 500 slags enzymatiske reaktioner i kroppen og er uundværlig for at opretholde normale livsaktiviteter. Det er ikke kun en central elektronbærer i energimetabolismeprocessen, men også et væsentligt substrat for aktivering af vigtige proteiner som Sirtuins og PARP'er, som bestemmer cellernes energiforsyning, reparationsevne og aldringshastighed. Med uddybningen af forskningen er NAD+ blevet et hot spot inden for anti-aging, behandling af stofskiftesygdomme og neurobeskyttelse, og dets niveauændring betragtes som en vigtig biomarkør for kroppens aldring og sundhedsstatus.
Den kemiske struktur og grundlæggende former for NAD+
NAD+ er et lille molekyle sammensat af to nukleotider, nemlig nikotinamidmononukleotid (NMN) og adenindinukleotid, og dets struktur indeholder nikotinamid (et derivat af vitamin B3), adenin, ribose og fosfatgrupper. Det findes hovedsageligt i to indbyrdes konverterbare former i celler: oxideret NAD+ og reduceret NADH. NAD+ er i en "tom" tilstand og kan acceptere elektroner, der genereres under metaboliske reaktioner, mens NADH er i en "fuld" tilstand, der bærer elektroner, som kan frigive elektroner i mitokondrie-respirationskæden for at fremme ATP-syntese. Cykluskonverteringen mellem NAD+ og NADH (NAD+ ↔ NADH) er kernen i celleenergiproduktion, og forholdet mellem NAD+/NADH påvirker direkte effektiviteten af energimetabolismen og redoxtilstanden af cellerPMC. Derudover kan NAD+ phosphoryleres for at danne NADP+, og dens reducerede form NADPH bruges hovedsageligt til antioxidativt stress og anabolske reaktioner, der kræver reducerende kraft, og i fællesskab opretholder balancen i celle-redox.

NAD+ er kernen i cellulær energimetabolisme
Den mest grundlæggende funktion af NAD+ er at tjene som et nøglecoenzym i cellulær energimetabolisme, ansvarlig for overførsel af elektroner i glykolyse, tricarboxylsyrecyklus (TCA-cyklus) og fedtsyreoxidationsprocesser. Når den menneskelige krop fordøjer og absorberer kulhydrater, fedtstoffer og proteiner, nedbrydes disse næringsstoffer til små molekyler og kommer ind i mitokondrierne. På dette tidspunkt accepterer NAD+ kontinuerligt hydrogenioner og elektroner fjernet under nedbrydningsprocessen og omdannes til NADH. NADH transporterer derefter disse højenergielektroner til den mitokondrielle elektrontransportkæde, og gennem en række redoxreaktioner fremmer det endelig syntesen af ATP, cellernes direkte energivaluta. Denne proces giver mere end 90 % af den energi, der kræves til livsaktiviteter, og understøtter grundlæggende fysiologiske funktioner som hjerteslag, hjernetænkning, muskelsammentrækning og celledeling. Uden tilstrækkelig NAD+ kan celler ikke omdanne mad til energi, og alle livsaktiviteter vil blive blokeret, hvilket fuldt ud afspejler den uerstattelige betydning af NAD+.
NAD+ dominerer DNA-reparation og genomisk stabilitet
DNA-skader er en uundgåelig begivenhed i cellelivets proces, og rettidig reparation er nøglen til at opretholde genomisk stabilitet og forhindre cellemutation og aldring. NAD+ spiller en central rolle i denne proces som et væsentligt substrat for Poly (ADP-ribose) Polymerase (PARP). Når DNA-enkeltstrengs- eller dobbeltstrengsbrud opstår, aktiveres PARP hurtigt og forbruger en stor mængde NAD+ for at syntetisere ADP-ribosekæder, som rekrutterer og aktiverer en række DNA-reparationsproteiner for at fuldføre reparationen af beskadigede steder. Samtidig er NAD+ også en nødvendig cofaktor for Sirtuins-proteinfamilien (inklusive SIRT1, SIRT3, SIRT6 osv.). Sirtuiner, kendt som "longevity proteiner", er afhængige af NAD+ for at udøve deacetyleringsaktivitet, regulere cellecyklus, hæmme celleapoptose, øge cellestressresistens og yderligere opretholde stabiliteten af kromosomer og gener. Undersøgelser har bekræftet, at manglen på NAD+ vil føre til et fald i PARP og Sirtuins aktiviteter, hvilket resulterer i akkumulering af DNA-skader, accelererer celleældning og øger risikoen for relaterede sygdomme.

NAD+ regulerer aldring og aldersrelaterede sygdomme
Et stort antal undersøgelser har bekræftet, at niveauet af NAD+ i forskellige væv og organer hos pattedyr falder signifikant med alderen. Forskning fra Harvard Medical School viser, at efter en alder af 25 falder den menneskelige krops NAD+ niveau med en hastighed på 12% til 15% om året; i en alder af 40, er det kun omkring 50 % af det i en alder af 20; i en alder af 60, falder det til 20% til 30%. Dette progressive fald er tæt forbundet med forekomsten af aldring og aldringsrelaterede sygdomme. Lave NAD+ niveauer fører til svækket mitokondriefunktion, reduceret energiproduktion, øget oxidativt stress og nedsat DNA-reparationskapacitet, som igen udløser en række ældningsmanifestationer såsom træthed, hukommelsestab, hudafslapning og metaboliske forstyrrelser. Derudover er faldet af NAD+ også forbundet med patogenesen af mange kroniske sygdomme, herunder type 2-diabetes, hjerte-kar-sygdomme, neurodegenerative sygdomme (Alzheimers sygdom, Parkinsons sygdom) og muskelatrofi. En undersøgelse offentliggjort i Nature Aging (2025) påpegede, at genoprettelse af NAD+-niveauer kan forbedre mitokondriefunktionen, beskytte neuroner og forsinke udviklingen af aldersrelaterede sygdomme. En anden undersøgelse i Cell Metabolism (2020) bekræftede, at NAD+ precursor-tilskud kan vende aldringsrelateret muskelatrofi og forbedre fysisk udholdenhed.

Biosynteseveje og tilskudsstrategier for NAD+
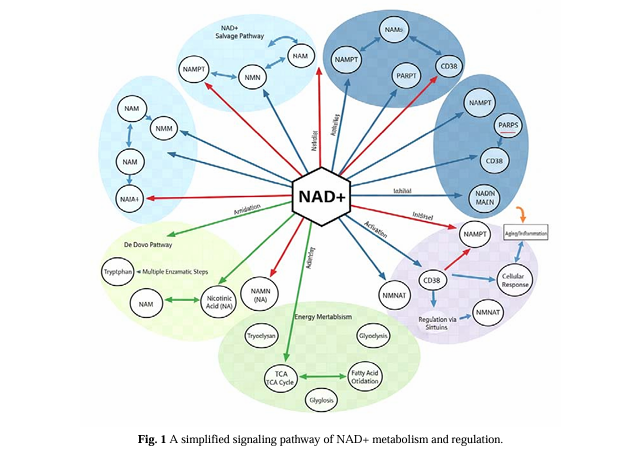
Den menneskelige krop syntetiserer hovedsageligt NAD+ gennem to veje: de novo syntesevej og redningsvejPMC. De novo syntesevejen starter fra tryptofan og afsluttes gennem flere enzymatiske reaktioner med lav effektivitet PMC. Bjærgningsvejen er hovedvejen for kroppen til at generere NAD+, som bruger nikotinamid (NAM), nikotinamidribosid (NR), nikotinamidmononukleotid (NMN) og andre forstadier til at syntetisere NAD+ gennem en række reaktioner, hvoriblandt nikotinamidphosphoribosyltransferase (NAMP.T) enzymet rate-PM (NAMP.T). Med alderen falder aktiviteten af NAMPT, og nedbrydningen af NAD+ (hovedsageligt medieret af CD38-enzym) øges, hvilket fører til et kontinuerligt fald i NAD+-niveauerPMC. På nuværende tidspunkt omfatter de vigtigste måder at øge NAD+-niveauer i kroppen på at supplere NAD+-prækursorer (såsom NMN, NR), hæmme CD38-enzymaktivitet og øge NAMPT-aktivitet. Blandt dem kan NMN og NR, som direkte forløbere for NAD+, effektivt omdannes til NAD+ efter indtræden i celler, og er blevet de mest undersøgte og anvendte kosttilskudsingredienser. Kliniske undersøgelser har vist, at fornuftigt tilskud af NAD+-prækursorer effektivt kan øge kroppens NAD+-niveau, forbedre energistofskiftet, øge træningskapaciteten, forbedre søvnkvaliteten og lindre kognitiv tilbagegang.
Konklusion
Sammenfattende er NAD+ (Nicotinamide Adenine Dinukleotid) et kerne-coenzym, der opretholder livsaktiviteter, der integrerer energimetabolisme, DNA-reparation, aldringsregulering og sygdomsforsvar. Det er ikke kun cellernes "kraftmotor", der er ansvarlig for at omdanne mad til energi, men også "reparatøren" af gener, der opretholder genomets stabilitet; det er også en "regulator" af aldring, og dets niveauændringer bestemmer direkte hastigheden af celleældning og kroppens sundhedsstatus. Faldet i NAD+-niveauet er en vigtig årsag til aldring og kroniske sygdomme, og en rimelig genoprettelse af NAD+-niveauet er blevet en nøglestrategi til at fremme sund aldring og forebygge relaterede sygdomme. Med det fortsatte gennembrud af videnskabelig forskning vil NAD+ spille en større rolle inden for sundhedspleje og klinisk medicin, hvilket giver nyt håb for menneskers sundhed og lang levetid.
Posttid: 2026-04-16
