Phosphorylering påvirker alle aspekter af cellulært liv, og proteinkinaser påvirker alle aspekter af intracellulære kommunikationsfunktioner ved at regulere signalveje og cellulære processer. Imidlertid er afvigende fosforylering også årsagen til mange sygdomme; Især kan muterede proteinkinaser og fosfataser forårsage mange sygdomme, og mange naturlige toksiner og patogener har også en virkning ved at ændre phosphoryleringsstatus for intracellulære proteiner.
Phosphorylering af serin (Ser), threonin (THR) og tyrosin (TYR) er en reversibel proteinmodifikationsproces. De er involveret i reguleringen af mange cellulære aktiviteter, såsom receptorsignalering, proteinforening og segmentering, aktivering eller inhibering af proteinfunktion og endda celleoverlevelse. Fosfater er negativt ladet (to negative ladninger pr. Fosfatgruppe). Derfor ændrer deres tilsætning egenskaberne ved proteinet, som normalt er en konformationel ændring, hvilket fører til en ændring i proteinets struktur. Når fosfatgruppen fjernes, vender proteinets konformation tilbage til dets oprindelige tilstand. Hvis de to konformationelle proteiner udviser forskellige aktiviteter, kan phosphorylering fungere som en molekylær switch for proteinet til at kontrollere dets aktivitet.
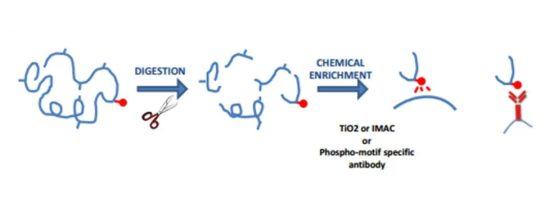
Mange hormoner regulerer aktiviteten af specifikke enzymer ved at øge phosphoryleringstilstanden for serin (Ser) eller threonin (THR) -rester og tyrosin (Tyr) phosphorylering kan udløses af vækstfaktorer (såsom insulin). Fosfatgrupperne af disse aminosyrer kan hurtigt fjernes. Således fungerer SER, THR og TYR som molekylære afbrydere i reguleringen af cellulære aktiviteter, såsom tumorproliferation.
Syntetiske peptider spiller en meget nyttig rolle i studiet af proteinkinasesubstrater og interaktioner. Der er dog nogle faktorer, der hindrer eller begrænser tilpasningsevnen af phosphopeptidsynteseteknologi, såsom manglende evne til at opnå fuld automatisering af fastfasesyntese og manglen på praktisk forbindelse med standardanalytiske platforme.
Den platformbaserede peptidsyntese og phosphoryleringsmodifikationsteknologi overvinder disse begrænsninger, mens den forbedrer synteseffektivitet og skalerbarhed, og platformen er velegnet til undersøgelse af proteinkinasesubstrater, antigener, bindingsmolekyler og hæmmere.
Posttid: 2025-07-02
