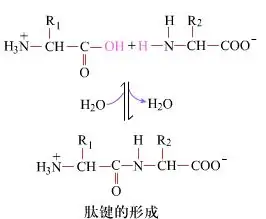
På overfladen er dannelsen af peptidbindinger, der giver dipeptider, en simpel kemisk proces. Dette betyder, at de to aminosyrekomponenter er forbundet med en peptidbinding, en amidbinding, mens den er dehydreret.
Dannelse af peptidbinding er aktivering af en aminosyre under milde reaktionsbetingelser. (A) Carboxylgruppe, anden aminosyre (B) Den nukleofile aktiverede carboxylgruppe danner derefter dipeptidet (A-B). "Hvis carboxylkomponenten (A) ikke er beskyttet, kan dannelsen af peptidbindingen ikke kontrolleres." Biprodukter, såsom lineære og cykliske peptider, kan blandes med målforbindelser A-B. Derfor skal alle funktionelle grupper, der ikke er involveret i dannelse af peptidbinding, beskyttes på en midlertidigt reversibel måde under peptidsyntese.
Så peptidsyntese - dannelsen af hver peptidbinding - involverer tre trin med aggregering.
Det første trin er at fremstille nogle aminosyrer, der har brug for beskyttelse, og den zwitterioniske struktur af aminosyrer findes ikke længere.
Det andet trin er en totrinsreaktion til dannelse af peptidbindinger, hvor carboxylgruppen af den N-beskyttede aminosyre først aktiveres til det aktive mellemprodukt, og derefter dannes peptidbindingen. Denne koblede reaktion kan forekomme enten som en et-trins reaktion eller som to sekventielle reaktioner.
Det tredje trin er den selektive fjernelse eller fuldstændig fjernelse af den beskyttende base. Selvom al fjernelse kun kan forekomme, er det også nødvendigt med beskyttelsesgrupper, når alle peptidkæder er samlet, også påkrævet selektiv fjernelse af beskyttelsesgrupper for at fortsætte peptidsyntesen.
Fordi 10 aminosyrer (SER, THR, TYR, ASP, GLU, Lys, Arg, His, His, SEC og Cys) indeholder sidekæde -funktionelle grupper, som kræver selektiv beskyttelse, hvilket gør peptidsyntese mere kompliceret. Midlertidige og semi-permanente beskyttelsesbaser skal skelnes på grund af de forskellige krav til selektivitet. Midlertidige beskyttelsesgrupper bruges i det næste trin til at afspejle den midlertidige beskyttelse af aminosyre eller carboxylfunktionelle grupper. Semi-permanente beskyttelsesgrupper fjernes uden at forstyrre allerede dannede peptidbindinger eller aminosyresidekæder, undertiden under syntese.
"Ideelt set skal aktivering af carboxylkomponenten og efterfølgende dannelse af peptidbindinger (koblingsreaktioner) være hurtige uden racemisk dannelse af racemisk eller biprodukt, og molære reaktanter skal påføres for at opnå høje udbytter." Desværre opfylder ingen af de kemiske koblingsmetoder disse krav, og få er egnede til praktisk syntese.
Under peptidsyntese er de funktionelle grupper, der er involveret i forskellige reaktioner, normalt knyttet til det manuelle center, hvor glycin er den eneste undtagelse, og der er en potentiel risiko for rotation.
Det sidste trin i peptidsyntesecyklussen er fjernelse af alle beskyttende grupper. Selektiv fjernelse af beskyttelsesgrupper er vigtig for peptidkædeforlængelse ud over kravet om fuldstændig fjernelse af beskyttelse i dipeptidsyntese. Syntetiske strategier skal planlægges omhyggeligt. Afhængigt af det strategiske valg kan N selektivt fjerne a-amino- eller carboxylbeskyttelsesgrupperne. Udtrykket "strategi" henviser til sekvensen af kondensationsreaktioner af individuelle aminosyrer. Generelt er der en forskel mellem gradvis syntese og fragmentkondensation. Peptidsyntese (også kendt som "konventionel syntese") finder sted i opløsning. I de fleste tilfælde kan gradvis forlængelse af peptidkæden kun syntetiseres ved anvendelse af peptidkæden til at syntetisere kortere fragmenter. For at syntetisere længere peptider skal målmolekylerne segmenteres i passende fragmenter og bestemmes, at de kan minimere graden af differentiering ved C -terminalen. Når de individuelle fragmenter gradvist er samlet, vil målforbindelsen blive sammenføjet. Strategien for peptidsyntese inkluderer valg af det bedste og mest passende beskyttende fragment, og strategien for peptidsyntese inkluderer valg af den mest passende kombination af beskyttende baser og den bedste metode til fragmentkonjugering.
Posttid: 2025-07-02